EQUILIBRIO QUÍMICO. LEY DE LE CHATELIER
DEFINICIÓN DE EQUILIBRIO QUÍMICO
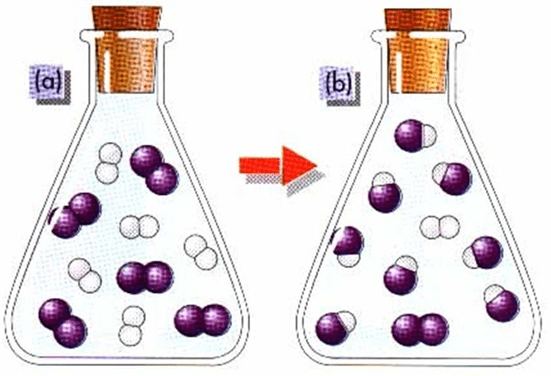
El equilibrio químico es el estado de una reacción química donde las concentraciones de los reactivos (sustancias iniciales) y las concentraciones de los productos (sustancias finales) no tienen ningún cambio neto.
El equilibrio químico se puede dar en dos situaciones:
1.- Cuando ya no hay más reactivos que puedan interactuar
2.- Cuando la producción de productos es exactamente la misma que la producción de reactivos en reacciones químicas reversibles.
FACTORES QUE AFECTAN EL EQUILIBRIO QUÍMICO
Los factores que pueden afectar el equilibrio químico de una reacción son:
1.- El cambio de concentración de un reactivo
2.- El cambio de temperatura del sistema
3.- El cambio de presión del sistema
Todos estos cambios pueden modificar el equilibrio químico y alterar las concentraciones entre reactivos y productos.
LEY DE LE CHATELIER
La Ley de Le Chatelier establece que, si en una reacción en equilibrio es perturbada desde el exterior, el sistema evoluciona con la intención de contrarrestar los efectos de dicha perturbación para llegar a un nuevo estado de equilibrio.
Mas ejemplos, ejercicios y preguntas clave de examen, en nuestras guías digitales.
-
 Guía UNAM Área 4 2023Producto rebajado$450.00
Guía UNAM Área 4 2023Producto rebajado$450.00 -
 Guía UNAM Área 3 2023Producto rebajado$450.00
Guía UNAM Área 3 2023Producto rebajado$450.00 -
 Guía UNAM Área 2 2023Producto rebajado$450.00
Guía UNAM Área 2 2023Producto rebajado$450.00 -
 Guía UNAM de Química Área 4-2023$80.00
Guía UNAM de Química Área 4-2023$80.00 -
 Guía UNAM de Química Área 3-2023$80.00
Guía UNAM de Química Área 3-2023$80.00 -
 Guía UNAM de Química Área 2-2023$90.00
Guía UNAM de Química Área 2-2023$90.00 -
 Guía UNAM Área 1 2023Producto rebajado$450.00
Guía UNAM Área 1 2023Producto rebajado$450.00 -
 Guía UNAM de Química Área 1-2023$80.00
Guía UNAM de Química Área 1-2023$80.00



