ESPECTROSCOPIA Y EL MODELO ATÓMICO DE BOHR
Toda la materia tiene una capacidad de absorber y emitir radiación electromagnética debido a las propiedades subatómicas del átomo.
Dependiendo el tipo de materia a considerar tendrá una emisión y una absorción de radiación diferente a otros tipos de materia.
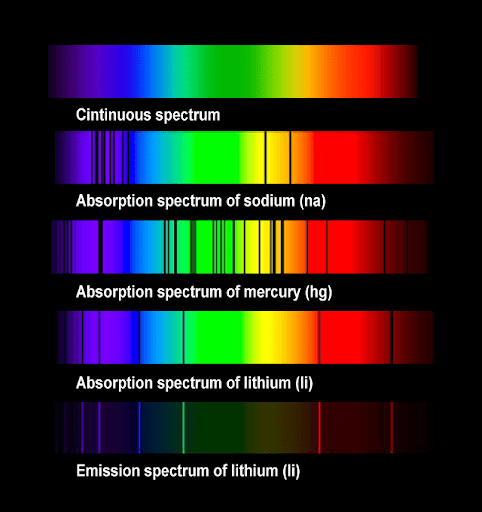
¿Qué es la espectroscopia?
La espectroscopia es la rama de la física que estudia esta propiedad de la materia de emitir y absorber radiación electromagnética.
Los diferentes tipos de radiación que emite un cuerpo se miden por la frecuencia y la longitud de onda de esta radiación.
Esta frecuencia y esta longitud de onda dependerá de unos fenómenos internos del átomo, que el modelo de Bohr puede explicar de la siguiente forma.
MODELO ATÓMICO DE BOHR
Cabe recordar que Thomson consideraba al átomo como una esfera llena de cargas positivas y negativas distribuidas en la superficie.
Después Rutherford llego a la conclusión que el núcleo concentraba la masa de átomo en el centro con carga positiva y que los electrones estaban alrededor del núcleo.
POSTULADOS DEL MODELO ATÓMICO DE BOHR
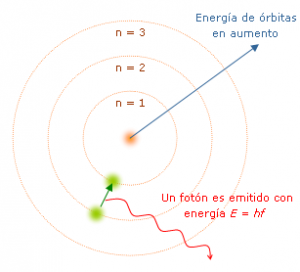
1.-Los electrones giran en orbitas circulares alrededor del núcleo del átomo sin irradiar energía.
2.-Solo existen ciertas orbitas en las cuales los electrones tienen permitido estar.
3.-El electrón solo emite o absorbe energía cuando pasa de una órbita permitida a otra. En dicho salto emite o absorbe un fotón cuya energía es la diferencia de energía entre ambos niveles
Mas ejemplos, ejercicios y preguntas clave de examen, en nuestras guías digitales.
-
 Guía UNAM Área 4 2023Producto rebajado$450.00
Guía UNAM Área 4 2023Producto rebajado$450.00 -
 Guía UNAM Área 3 2023Producto rebajado$450.00
Guía UNAM Área 3 2023Producto rebajado$450.00 -
 Guía UNAM Área 2 2023Producto rebajado$450.00
Guía UNAM Área 2 2023Producto rebajado$450.00 -
 Guía UNAM de Física Área 4-2023$90.00
Guía UNAM de Física Área 4-2023$90.00 -
 Guía UNAM de Física Área 3-2023$90.00
Guía UNAM de Física Área 3-2023$90.00 -
 Guía UNAM de Física Área 2-2023$90.00
Guía UNAM de Física Área 2-2023$90.00 -
 Guía UNAM Área 1 2023Producto rebajado$450.00
Guía UNAM Área 1 2023Producto rebajado$450.00 -
 Guía UNAM de Física Área 1-2023$90.00
Guía UNAM de Física Área 1-2023$90.00



