LA ENERGÍA Y LAS REACCIONES QUÍMICAS
CONCEPTOS INICIALES DE ENERGÍA Y LAS REACCIONES QUÍMICAS
DEFINICIÓN DE REACCIÓN QUÍMICA
Una reacción química es un fenómeno que se da cuando una o más sustancias tienen cambios químicos que provocan que se transformen en otras sustancias diferentes.
Para que las reacciones químicas se lleven a cabo, regularmente se requiere una cantidad de energía mínima llamada energía de activación con la cual la reacción química interactúa con su ambiente.
Es decir, en toda reacción química hay un intercambio de energía entre el sistema y su entorno.
Este fenómeno se divide en 3 pasos también llamado “reacción en cadena”
REACCIÓN EN CADENA
1.- Paso de iniciación donde están presentes los elementos a interactuar, reactivos (sustancias iniciales) y como resultado de esta interacción dan un intermediario reactivo.
2.- Pasos de propagación: Este intermediario reactivo reacciona con otra molécula estable para dar más productos y más intermediarios reactivos.
3.- Pasos de terminación: las reacciones colaterales destruyen a los intermediarios reactivos y tienden a disminuir o detener la reacción.
EL MECANISMO DE LA REACCIÓN QUÍMICA
El mecanismo de la reacción química es la descripción completa, paso a paso, de los enlaces que exactamente se rompen y de los que se forman para formar los productos derivados
ECUACIONES QUÍMICAS
Las ecuaciones químicas son los símbolos que utilizamos para representar a las reacciones químicas. Los elementos de las ecuaciones químicas son:
1.- Del lado izquierdo de la ecuación están los “reactivos”
2.- Del lado derecho están los productos
3.- En los dos lados de la ecuación anotamos las cantidades relativas que intervienen.
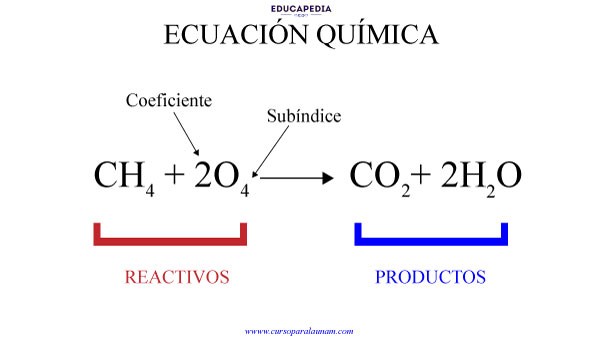
4.- Los coeficientes indica la cantidad del elemento presente y SI se pueden modificar para balancear la ecuación.
5.- Los subíndices indican el número de átomos de cada elemento presente y NO se pueden modificar para balancear la ecuación.
TERMODINÁMICA QUÍMICA
La termodinámica química es el estudio de los cambios de energía que acompañan a las transformaciones físicas y químicas.
PROCESO TERMODINÁMICO
Un proceso termodinámico es un proceso en el que un sistema con un estado inicial en equilibrio intercambia energía con su entorno para terminar en otro estado final en equilibrio.
CINÉTICA QUÍMICA
La cinética química es el estudio de la rapidez de las reacciones.
Próximos subtemas que marca la guía UNAM:
- 5.1 Reacciones químicas endotérmicas y exotérmicas.
- 5.2 Energía interna.
- 5.3 Entalpia.
- 5.4 Energía libre y espontaneidad.
- 5.5 Equilibrio químico: Ley de Chatelier
- 5.6 Velocidad de reacción y factores que influyen en ella.
Mas ejemplos, ejercicios y preguntas clave de examen, en nuestras guías digitales.
-
 Guía UNAM Área 4 2023Producto rebajado$450.00
Guía UNAM Área 4 2023Producto rebajado$450.00 -
 Guía UNAM Área 3 2023Producto rebajado$450.00
Guía UNAM Área 3 2023Producto rebajado$450.00 -
 Guía UNAM Área 2 2023Producto rebajado$450.00
Guía UNAM Área 2 2023Producto rebajado$450.00 -
 Guía UNAM de Química Área 4-2023$80.00
Guía UNAM de Química Área 4-2023$80.00 -
 Guía UNAM de Química Área 3-2023$80.00
Guía UNAM de Química Área 3-2023$80.00 -
 Guía UNAM de Química Área 2-2023$90.00
Guía UNAM de Química Área 2-2023$90.00 -
 Guía UNAM Área 1 2023Producto rebajado$450.00
Guía UNAM Área 1 2023Producto rebajado$450.00 -
 Guía UNAM de Química Área 1-2023$80.00
Guía UNAM de Química Área 1-2023$80.00